Pasti semua sudah tahu apa intan itu. Intan adalah salah satu bentuk isotop dari karbon dengan struktur geometri tetrahedral (sp3). Dalam keadaan murninya, intan tersusun atas atom-atom karbon yang saling berikatan sehingga terbentuklah jaringan kovalen raksasa. Setiap satuan kristalnya membentuk kisi face–centered cubic. Hal yang cukup menarik, meskipun intan merupakan salah satu mineral yang sangat kuat (Skala Mohs 10), mineral ini justru lebih tidak stabil dibandingkan dengan grafit secara termodinamika. Ini ditandai oleh entalpi pembentukan standar dari intan dan grafit sebesar $latex 0~{\rm kJ~mol}^{-1}$ dan $latex 1,90~{\rm kJ~mol}^{-1}$.
Pernah melihat warna-warni intan seperti intan hitam, coklat, kuning, atau merah? Penasaran kok bisa intan itu warna–warni? Warna dari intan itu sendiri bergantung pada tingkat kemurnian yang ada di dalamnya. Namun, sebelum bicara tingkat kemurnian intan, mari kita bahas terlebih dahulu beberapa hal mengenai cacat kristal!
Tidak ada yang sempurna. Pepatah ini sangat cocok dengan fenomena munculnya warna pada intan. Masih ingat hukum termodinamika III yang menyatakan hanya intan pada 0 K yang memiliki nilai entropi sebesar 0? Pada suhu normal tidak mungkin entropi suatu zat sebesar nol. Adanya nilai entropi suatu zat menandakan bahwa ada “ketidakteraturan” di dalam suatu zat. Demikian pula di dalam intan, adanya ketidakteraturan inilah yang menyebabkan cacat pada intan. Namun, cacat yang dimaksud di sini tidak sama dengan cacat pada manusia.
Ada tiga kategori besar dari cacat kristal, yaitu cacat titik, cacat garis, dan cacat bidang. Pada tulisan ini hanya akan dibahas tentang cacat titik saja. Dalam konsep cacat titik dikenal istilah Cacat Schottky dan Cacat Frenkel. Cacat Schottky ditandai oleh adanya kekosongan pada suatu titik kisi, sedangkan Cacat Frenkel merupakan keadaan di saat suatu atom kisi menyisipkan dirinya bukan pada tempat yang seharusnya.
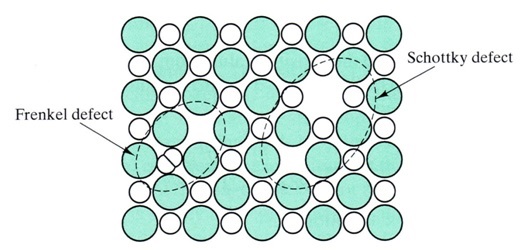
Karena adanya cacat ini, ion–ion lain seperti $latex {\rm Ca}^{2+}$, $latex {\rm Cd}^{2+}$, $latex {\rm Cu}^{2+}$, dan $latex {\rm CO}_3^{2-}$, yaitu ion-ion yang dapat memberi warna pada intan, itu bisa masuk kedalam tempat cacat intan. Jadi, jika kita melihat intan berwarna biru, kita bisa menyimpulkan bahwa intan tersebut memiliki kandungan ion tembaga $latex {\rm Cu}^{2+}$ atau Boron yang cukup banyak. Adanya pengotor dalam struktur intan dapat mengubah spektrum absorbsi intan.
Spektrum intan yang berubah akibat adanya pengotor tergantung pada jenis dan konsentrasi pengotor yang ada. Misalnya, intan kuning dan oranye mengandung unsur nitrogen; intan biru mengandung unsur boron; intan abu-abu, ungu, dan hijau mengandung unsur hidrogen. Intan hijau juga dapat disebabkan oleh radiasi alam, yang terjadi selama berjuta-juta tahun sehingga dapat mengubah struktur atom dalam intan dan spektrum absorpsi intan pun berubah. Intan merah muda, merah dan coklat dapat juga disebabkan oleh adanya deformasi plastik. Struktur atom karbon yang memutar selama pembentukan intan dalam tanah dapat mengubah spektrum absorpsi intan. Hal ini tampak pada intan sebagai garis urat yang menyerupai urat kayu. Garis inilah yang memberikan spektrum warna yang berbeda.

Bahan bacaan:
Penulis:
M. Al-Rizqi Dharma Fauzi, mahasiswa jurusan kimia, Universitas Airlangga.
Kontak: dertraum0127(at)gmail(dot)com.



