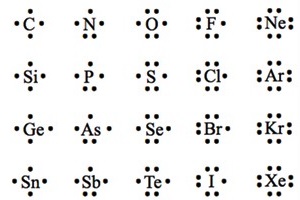Perhatikan dua gambar struktur molekul metana (CH4) berikut ini.
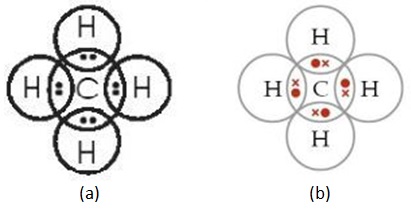
Barangkali ada yang berujar, keduanya sama-sama merupakan struktur Lewis dari molekul metana. Bila ada yang berujar demikian, itu tidaklah tepat. Banyak buku yang menyebutkan bahwa kedua gambar tersebut merupakan struktur Lewis untuk molekul metana. Perlu diketahui bahwa gambar (a) memang merupakan struktur Lewis untuk molekul metana. Lantas bagaimana dengan gambar (b)? Gambar (b) bukan struktur Lewis untuk molekul metana, akan tetapi struktur Linnett untuk molekul metana.
Gilbert Newton Lewis, atau yang lebih dikenal dengan Lewis, adalah kimiawan yang memprakarsai cara penggambaran struktur molekul dengan sederhana. Penggambaran struktur molekul tersebut menggunakan titik-titik yang menyatakan elektron valensi dari suatu atom.
Simbol Lewis atau lambang Lewis merupakan simbol suatu atom yang dikelilingi oleh titik-titik yang menyatakan elektron valensi dari atom tersebut. Ketika atom-atom membentuk molekul dengan ikatan kovalen akan terjadi perubahan jumlah elektron pada valensi masing-masing atom akibat adanya pemakaian bersama dua buah elektron oleh dua atom. Penggambaran struktur molekul yang dihasilkan akibat pembentukan ikatan tersebut didasarkan pada konsep simbol Lewis untuk gas mulia (duplet dan oktet).

Lantas, bagaimana dengan struktur molekul model Linnett? Bukankah sama saja dengan struktur molekul model Lewis? Struktur Linnett memang diilhami oleh ide Lewis. John Wilfrid Linnett memodifikasi model Lewis. Linnett mengusulkan agar membagi elektron oktet menjadi dua set dari empat elektron. Dalam setiap set elektron saling tolak-menolak sejauh mungkin.
Struktur molekul model Linnett memang jarang sekali terdengar dibandingkan struktur molekul model Lewis. Namun, untuk kejujuran ilmiah dalam pendidikan kimia, alangkah baiknya diinformasikan bahwa selain model Lewis ada juga model Linnett dalam penggambaran struktur molekul secara sederhana. Dengan demikian, struktur molekul model Linnett tidak lagi dikatakan struktur molekul model Lewis.
Bahan bacaan:
- Miessler, G. L., Fischer, J.P., and Tarr, D. A., 2014, Inorganic Chemistry, Pearson Education Inc., United States of America.
- Surdia, N. M., 1994. Ikatan dan Struktur Molekul, Depdikbud Dirjen Dikti Proyek Pembinaan dan Peningkatan Mutu Tenaga Kependidikan, Jakarta.
- Efendy, 2010, Teori VSEPR, Kepolaran, dan Gaya, Bayumedia Publishing, Malang.
Penulis:
Mahfudz Fauzi , Dosen Program Studi Pendidikan Kimia Universitas Lampung.
Kontak: m(dot)mahfudz(dot)fauzi(dot)s(at)gmail(dot)com.