Jika teman-teman belajar kimia, barangkali teman-teman akan familiar dengan kata “hidrogenasi”. Berasal dari kata hidrogen, reaksi hidrogenasi berarti reaksi kimia yang menggunakan hidrogen (H2) sebagai reaktan dengan senyawa organik. Melalui reaksi hidrogenasi, senyawa asam karboksilat, aldehid, dan keton akan menjadi senyawa alkohol sedangkan senyawa tak jenuh (seperti alkena dan alkuna) akan membentuk senyawa jenuh (seperti alkana).
Karena banyaknya jenis reaksi hidrogenasi, reaksi ini banyak dimanfaatkan oleh peneliti dan sektor industri untuk mensintesis senyawa yang diinginkan dan bernilai jual tinggi. Reaksi hidrogenasi bersifat sensitif terhadap kondisi reaksi, seperti temperatur, tekanan, dan material katalis. Temperatur, tekanan, dan material katalis yang berbeda memiliki mekanisme dan produk yang berbeda pula. Reaksi hidrogenasi akan berjalan jika katalis yang digunakan ialah logam seperti Ni, Pd dan Pt, tetapi hidrogenasi tidak akan terjadi jika menggunakan katalis logam oksida seperti NiO, PdO, dan PtO.
Namun, apa yang terjadi jika hidrogenasi dilakukan pada suatu senyawa yang terdapat ikatan C=C (alifatik) dan C=O (gugus karbonil) terkonjugasi (atau kedua ikatan ganda tersebut diselingi oleh ikatan tunggal)? Tentu kedua ikatan ganda tersebut pasti akan terhidrogenasi, jika parameter reaksi tidak dimodifikasi dengan tepat.
Maki-Arvela dkk. pada tahun 2005 melaporkan bahwa ternyata ikatan C=C secara termodinamika lebih mudah terhidrogenasi dibandingkan dengan ikatan C=O, dengan selisih sekitar 35 kJ/mol. Selain itu, Musolino dkk. pada tahun 2003 melaporkan adanya isomerisasi senyawa enol yang terbentuk menjadi senyawa keton yang tidak diharapkan.
Berangkat dari penelitian-penelitian tersebut, menjadi sebuah tantangan besar jika kita ingin menghidrogenasi ikatan C=O pada senyawa yang terkonjugasi dengan ikatan C=C. Hal inilah yang saat ini menjadi salah satu topik yang menarik minat para peneliti untuk dikembangkan. Oleh karena itu, diperlukan berbagai strategi khusus agar reaksi hidrogenasi yang dilakukan menjadi lebih selektif terhadap ikatan C=O.
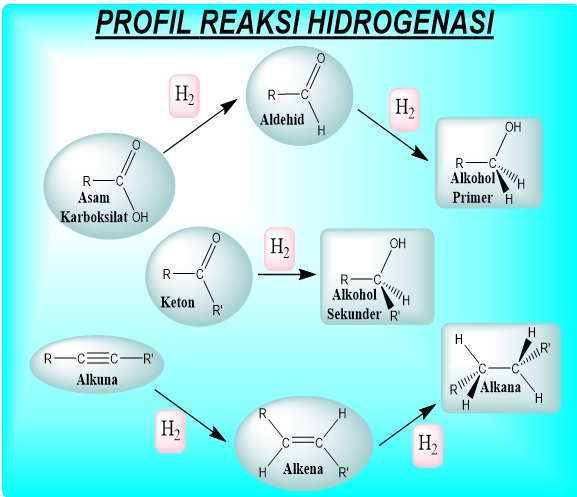
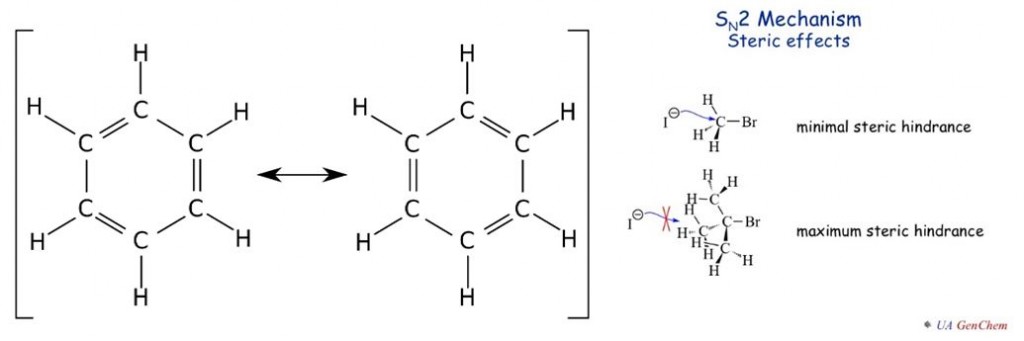
 Terdapat berbagai macam strategi yang telah dikembangkan oleh peneliti untuk menghidrogenasi gugus karbonil di senyawa alifatik, yaitu menggunakan senyawa yang memiliki kestabilan ikatan C=C tinggi. Asam benzoat misalnya, ikatan C=C yang terkonjugasi satu sama lain pada struktur gugus benzil memungkinkan ikatan tersebut untuk beresonansi. Resonansi merupakan suatu bentuk representasi tingginya kestabilan akibat adanya delokalisasi elektron dalam suatu molekul.
Terdapat berbagai macam strategi yang telah dikembangkan oleh peneliti untuk menghidrogenasi gugus karbonil di senyawa alifatik, yaitu menggunakan senyawa yang memiliki kestabilan ikatan C=C tinggi. Asam benzoat misalnya, ikatan C=C yang terkonjugasi satu sama lain pada struktur gugus benzil memungkinkan ikatan tersebut untuk beresonansi. Resonansi merupakan suatu bentuk representasi tingginya kestabilan akibat adanya delokalisasi elektron dalam suatu molekul.
Akibat adanya resonansi, ikatan C=C menjadi sulit untuk dihidrogenasi. Selain resonansi, strategi untuk mencegah terjadinya hidrogenasi ikatan C=C ialah menggunakan senyawa yang memiliki struktur meruah (bulky) pada ikatan C=C. Keadaan ini mengakibatkan hidrogenasi ikatan C=C akan terhalang dan tidak memungkinkan terjadinya hidrogenasi ikatan C=C. Kondisi ini biasa disebut dengan efek sterik.
Efek sterik tidak hanya dapat diaplikasikan ke reaktan saja. Penggunaan katalis yang memiliki efek sterik juga mampu mengurangi terjadinya hidrogenasi pada ikatan C=C. Jika katalis logam Ni memiliki sifat hidrogenasi yang tinggi terhadap ikatan C=C, penggunaan ligan dengan strutur yang meruah juga dapat mengurangi kemampuan hidrogenasinya. Ditambahkannya ligan, maka struktur kompleks Ni akan terbentuk, sehingga selektifitas katalisnya akan meningkat akibat adanya efek sterik.
Penambahan material pengemban (supporting material) seperti zeolit, TiO2, Al2O3, hidrotalsit, dan lain-lain juga telah terbukti mampu meningkatkan selektifitas hidrogenasi katalis terhadap ikatan C=O (gugus karbonil). Maki-Arvela dkk. pada tahun 2002 melaporkan bahwa katalis logam Ni yang ditambahkan dengan material pengemban Al2O3 (dinotasikan sebagai Ni/Al2O3) mampu menghidrogenasi sitral menjadi geraniol dengan selektifitas sebesar 94%, dibanding tanpa Al2O3 yang tidak menghasilkan produk geraniol. Berbagai macam modifikasi katalis inilah yang banyak menarik minat peneliti kimia katalis untuk terus mengembangkan katalis agar menghasilkan performa yang tinggi.
Penambahan logam yang memiliki berbagai macam sifat keasaman, oksofilisitas, dan elektropositifitas yang tinggi ke logam utama merupakan fokus yang akan dipaparkan dalam artikel kali ini. Lho, logam bisa bersifat asam ya? Barangkali itu yang mungkin muncul di benak teman-teman. Logam yang besifat asam di sini bukan berarti logam yang mengandung H+. Konsep keasaman yang melihat H+ sebagai parameter utama itu ialah konsep asam-basa Bronsted-Lowry, ketika pendonor H+ besifat asam sedangkan akseptor H+ bersifat basa.
Namun, ada konsep keasaman lain yang lebih penting dan perlu teman-teman ketahui, yaitu konsep asam-basa Lewis. Konsep ini melihat elektron sebagai fokusnya. Senyawa yang mendonorkan pasangan elektronnya bersifat basa, sebaliknya penerima pasangan elektron bersifat asam. Dengan demikian, logam yang bersifat asam ialah logam yang mampu menerima pasangan elektron dan pendonornya. Logam golongan IIIA (seperti B, Al, Ga, In, dan Tl) merupakan contoh yang paling umum dari logam yang bersifat asam.
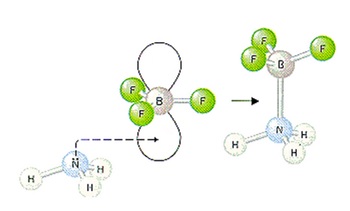
Yuk, coba kita jabarkan bagaimana bentuk konfigurasi elektron dari logam boron, 5B = 1s2, 2s2, 2p1. Diketahui bahwa elektron terakhir dari konfigurasi (disebut dengan elektron valensi) jatuh pada 2p1, yang berarti kulit ke-2 dan di orbital p. Orbital p memiliki 3 buah orientasi ruang, yaitu px, py dan pz. Jika membentuk ikatan, 1 elektron di 2s akan pindah ke salah satu orbital 2p (hal ini biasa disebut dengan hibridisasi) sehingga ada 3 elektron yang tidak berpasangan di 1 orbital s dan 2 di orbital p.
Kondisi inilah yang menyebabkan boron mampu membentuk 3 ikatan kovalen agar mencapai kestabilan tertingginya. Mengingat masih ada 1 orbital kosong p yang belum terisi elektron, maka keadaan inilah yang memungkinkan senyawa lain mendonorkan pasangan elektron bebasnya hingga membentuk ikatan kovalen koordinasi. Kemampuan boron menerima pasangan elektron dari senyawa lain inilah yang menyebabkan boron bersifat asam.
Kemudian, apa itu oksofilik? Berasal dari kata okso- yang berasal dari kata oksigen sedangkan –filik berarti suka. Artinya, logam dengan sifat oksofilik kurang lebih berarti logam yang suka berinteraksi dengan atom oksigen. Bagaimana dengan elektropositif? Mungkin kita lebih familiar dengan istilah elektropositif bukan? Jika sifat elektronegatif merupakan kemampuan untuk menarik elektron, maka elektropositif berarti kemampuan sebaliknya.
Sifat elektropositif yang mengakibatkan terbentuknya muatan positif, sifat oksofilik yang mengakibatkan tertariknya unsur O, dan sifat asam yang menyediakan orbital kosong ketika berinteraksi dengan unsur O, maka diharapkan ikatan C=O dapat terikat kuat pada logam dan gugus karbonil tersebut menjadi lebih mudah terhidrogenasi. Terdapat beberapa logam yang memiliki 3 sifat tersebut, di antaranya Co, Fe, dan Sn.
Logam tambahan yang dipilih pada paparan kali ini ialah Fe, karena selain memiliki nilai ekonomi yang murah, dan ketersediaan yang melimpah, logam Fe juga dikenal memiliki sifat kemagnetan yang tinggi. Diharapkan pemisahan antara padatan dan larutan ketika reaksi selesai menjadi lebih mudah, cukup menggunakan magnet padatan katalis akan terpisah secara otomatis. Sedangkan logam utama hidrogenasi yang dipilih di sini ialah Ni, karena memiliki nilai ekonomi yang lebih rendah dibanding Pd dan Pt.
Seperti yang penulis utarakan dalam tulisan sebelumnya, di majalah 1000guru edisi Februari 2015, paduan Ni-Fe dapat dibuat ke dalam bentuk nanoflower. Bentuk yang unik, metode pemisahan yang mudah, dan nilai ekonomis yang tinggi merupakan berbagai kelebihan yang dimiliki katalis paduan Ni-Fe. Proses pembuatan paduan ini adalah dengan metode pengendapan dan hidrotermal sederhana. NiCl2 dan FeCl3 digunakan sebagai prekursor dan NaOH sebagai pengendap.
Campuran NiCl2 dan FeCl3 yang telah dilarutkan dengan air diendapkan dengan NaOH, menjadi endapan Ni(OH)2 dan Fe(OH)3. Proses hidrotermal berfungsi untuk membentuk logam oksida (NiO dan Fe2O3) dengan melepas H2O sebagai produk sampingnya. Logam oksida tersebut kemudian direduksi dengan hydrogen pada temperatur tinggi.
Reaksi-reaksi yang terjadi dalam proses pembuatan katalis nanoflower paduan Ni-Fe dapat dilihat dalam diagram berikut.
Proses pelarutan:
NiCl2(s) + H2O(l) -> NiCl2(aq) -> Ni2+(aq) + 2Cl–(aq)
FeCl3(s) + H2O(l) -> FeCl3(aq) -> Fe3+(aq) + 3Cl–(aq)
Proses pengendapan:
Ni2+(aq) + 2Cl–(aq) + 2NaOH(aq) -> Ni(OH)2(s) + 2NaCl(aq)
Fe2+(aq) + 3Cl–(aq) + 3NaOH(aq) -> Fe(OH)3(s) + 3NaCl(aq)
Proses hidrotermal:
Ni(OH)2(s) -> NiO(s) + H2O(l)
Proses reduksi:
2Fe(OH)3(s) -> Fe2O3(s) + 3H2O(l)
6NiO(s) + Fe2O3(s) + 9H2(s) -> 2Ni3Fe(s) + 9H2O(l)

Katalis nanoflower paduan Ni-Fe yang diperoleh kemudian diaplikasikan untuk reaksi hidrogenasi gugus karbonil secara selektif pada senyawa furfural. Reaksi dilakukan dalam sistem cair, dengan reaktor sistem batch. Pada sistem tidak ada aliran cairan yang masuk dan keluar seperti yang terjadi pada reaktor sistem kontinu. Gas hidrogen dimasukkan ke dalam sistem reaktor pada tekanan tertentu dan temperatur tertentu. Hasil yang diperoleh dianalisis menggunakan instrumen kromatografi gas.

Senyawa yang memiliki ikatan C=C dan C=O terkonjugasi seperti furfural memiliki tiga kemungkinan produk reaksi hidrogenasi. Produk 1 diperoleh ketika ikatan C=O terhidrogenasi, sedangkan jika C=C terhidrogenasi, hasil yang diperoleh ialah produk 2. Produk 3 diperoleh jika baik ikatan C=C dan C=O terhidrogenasi. Ketiga senyawa tersebut digunakan untuk melihat distribusi produk yang dihasilkan dari hasil reaksi katalitik menggunakan katalis paduan logam Ni-Fe.
Berdasarkan data yang diperoleh terlihat bahwa katalis logam Ni memiliki tingkat hidrogenasi yang sangat tinggi, dengan nilai konversi yang mencapai 100%, tetapi nilai selektivitas terhadap produk nomor 1 sangat rendah (hanya sekitar 6,9%). Sebaliknya, katalis logam Fe tidak menunjukkan aktivitas katalitik yang terjadi dalam reaksi hidrogenasi. Hal ini dapat dilihat dari nilai konversinya 0%. Namun, ketika logam Fe dipadukan dengan logam Ni, selektivitas yang diperoleh untuk mendapat produk 1 meningkat secara signifikan.
Selektivitas di atas 90% diperoleh ketika logam Fe dipadukan dengan logam Ni dengan berbagai macam rasio Ni/Fe. Hal ini menandakan bahwa paduan logam katalis Ni-Fe sangat efektif digunakan untuk menghidrogenasi gugus karbonil pada furfural secara selektif.

Setelah mengetahui latar belakang, cara membuat dan hasil reaksi yang diperoleh, pertanyaan yang muncul sekarang ialah bagaimana jalannya mekanisme reaksi sehingga produk 1 (furfural alcohol) bisa dihasilkan. Sayang teknologi femtochemistry seperti yang telah diutarakan oleh penulis dalam majalah1000guru edisi bulan April 2015 tidak tersedia, sehingga mekanisme yang diajukan hanyalah perkiraan dari beberapa hasil reaksi yang telah dilakukan sebelumnya.
Berdasarkan skema mekanisme reaksi yang diajukan di atas, terlihat bahwa logam Ni mampu memecah hidrogen secara homolitik menjadi spesies hidrida (H–), yang kemudian terkoneksi pada permukaan Ni. Spesies inilah yang berfungsi untuk menghidrogenasi ikatan C=C dan C=O pada furfural. Sifat elektropositif yang dimiliki oleh logam Fe membuat muatan parsial positif terbentuk pada Fe akibat donasi kerapatan elektron dari Fe ke Ni. Muatan parsial positif inilah yang memperkuat interaksi antara atom O pada ikatan C=O dengan logam Fe, selain tingginya sifat oksofilik dan keasaman yang dimiliki oleh logam Fe.
Oleh karena kuatnya interaksi yang terbentuk, ikatan C=O menjadi lebih mudah terhidrogenasi dibandingkan dengan ikatan C=C pada furfural. Selama ini, katalis hidrogenasi gugus karbonil yang telah diaplikasikan untuk sektor industri ialah katalis paduan Cu-Cr. Seperti yang kita ketahui bahwa logam Cr memiliki tingkat toksisitas yang tinggi terhadap lingkungan, sehingga logam seperti ini perlu dihindari. Berdasarkan data di atas, katalis nanoflower paduan Ni-Fe memiliki potensi yang tinggi untuk dapat diterapkan ke sektor industri. Namun masih diperlukan beberapa kajian lebih lanjut sebelum diaplikasikan ke sektor industri.
Kajian seperti scale-up (peningkatan skala), reusability (pengulangan reaksi), dan aplikasi ke reactor flow system (reaktor dengan sistem kontinu) perlu dipelajari agar bisa diaplikasikan ke sektor industri dengan baik. Hasil riset yang kita peroleh selama ini hendaknya bisa diaplikasikan ke sektor industri agar bermanfaat dan dapat dinikmati oleh masyarakat secara luas. Untuk mewujudkan hal tersebut, dibutuhkan kerja sama yang solid antara sektor industri dengan kalangan akademisi, agar hasil riset yang mereka peroleh tidak hanya berhenti sebagai artikel. Semoga Indonesia ke depannya dapat menjadi negara yang lebih maju melalui berbagai hasil riset yang bemanfaat bagi masyarakat banyak melalui pengembangannya ke sektor industri.
Bahan bacaan:
- G. Musolino, P. De Maio, A. Donato, dan R. Pietropaolo. 2004. Hydrogenation Versus Isomerization in α, β-unsaturated Alcohols Reactions over Pd/TiO2 Catalysts. J. Mol. Catal. A: Chem. 208. 219-224
- Maki-Arvela. L. P. Tiainen. A. Kalantar, R. Sjoholm, T. K Rantakyla, E. Laine, T. Salmi, dan D. Yu. Murzin. 2002 . Liquid Phase Hydrogenation of Citral: Suppression of Side Reactions. Appl. Catal. A. 237. 181.
- Maki-Arvela, J. Hajek, T. Salmi, D. Yu. Murzin. 2005. Chemoselective Hydrogenation of Carbonyl Compound Over Heterogeneous Catalysts. Appl. Catal. A: General. 292. 1-49.
- http://en.wikipedia.org/wiki/Resonance_(chemistry)
- http://www.infoescola.com/quimica/femtoquimica/
- http://www.uni-heidelberg.de/fakultaeten/chemgeo/pci/motzkus/
- http://majalah1000guru.net/2015/02/menyimak-indahnya-material-nanoflower/
- http://majalah1000guru.net/2015/04/mengenal-femtochemistry/
Penulis:
Wahyu Satpriyo Putro, mahasiswa master di Department of Applied Chemistry and Biotechnology, Chiba University, Jepang. Kontak: wahyu_kim07(at)yahoo(dot)com.



