Hidrogen merupakan unsur yang paling sederhana dan melimpah di alam semesta. Unsur hidrogen terdiri atas satu proton dan satu elektron dan tak perlu dijelaskan lebih lanjut bahwa keberadaan hidrogen di bumi adalah sebagai air (H2O). Karena sifat kepolarannya dapat berubah dengan mudah antara hidrida (H–), atom (H), dan proton (H+), hidrogen juga dapat membentuk berbagai senyawa dengan banyak unsur, termasuk dengan oksigen dan karbon. Oleh karena itu, hidrogen merupakan unsur yang sangat penting dalam kehidupan manusia.
Berdasarkan klasifikasi posisi unsur dalam tabel periodik dan karakter ikatannya, hidrida biner dapat dibagi menjadi beberapa kelompok, antara lain: (1) hidrida alkali atau hidrida salin, (2) hidrida kovalen molekular, (3) hidrida molekular kompleks, dan (4) hidrida logam. Dalam artikel kali ini, kita akan mengulas lebih jauh mengenai berbagai macam hidrida tersebut dan salah satu aplikasi penting hidrida untuk penyimpanan gas hidrogen yang sedang dikembangkan pada beberapa negara maju dalam industri otomotif di masa depan.
***
Macam-macam hidrida
1. Hidrida salin
Hidrida salin merupakan senyawa ionik dari material alkali tanah di blok s pada tabel periodik yang analog dengan halida sehingga dapat pula disebut hidrida alkali. Beberapa contoh khas dari hidrida kelompok ini, antara lain:
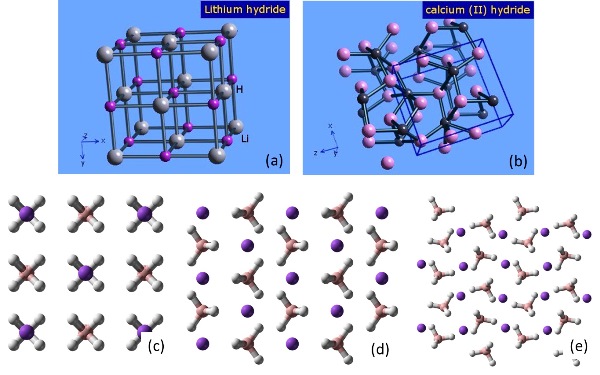
(i) Litium hidrida (LiH), yaitu senyawa kristalin tak berwarna dengan titik leleh sekitar 68$latex ^{\circ}\textrm{C}$ yang mana Li+ dan H– membentuk kristal berstruktur natrium klorida (NaCl). Pelepasan kuantitatif gas hidrogen di anoda saat dilakukan elektrolisis garam leburnya menyebabkan terbentuknya hidrida karena air bereaksi dengan hebat dengan lithium hidrida yang kemudian membebaskan gas hidrogen. Oleh karena senyawa ini agak melarut dalam eter, hidrida ini banyak digunakan sebagai pereduksi di kimia organik.
(ii) Kalsium hidrida (CaH$latex _2$), yaitu padatan kristalin tak berwarna dengan titik leleh mencapai 816$latex ^{\circ}\textrm{C}$. Seperti halnya LiH, CaH$latex _2$ juga bereaksi hebat dengan air dan membebaskan gas hidrogen. Hidrida ini digunakan sebagai pembentuk gas hidrogen atau bahan dehidrator untuk pelarut organik atau dapat juga digunakan sebagai reduktor.
(iii) Natrium tetrahidroborat (NaBH$latex _4$), yaitu senyawa padatan kristalin berwarna putih yang terdekomposisi pada suhu di atas 400$latex ^{\circ}\textrm{C}$ dan biasanya disebut juga dengan natrium borohidrida. Padatan ini larut dalam air yang kemudian melepaskan gas hidrogen pada saat terdekomposisi. Padatan ini digunakan sebagai bahan pereduksi untuk senyawa anorganik dan organik dan dapat pula digunakan pada proses preparasi kompleks hidrida.
2. Hidrida molekular
Semua hidrida kecuali hidrida karbon (metana) dan oksigen (air) adalah gas beracun dengan kereaktifan sangat tinggi dan harus ditangani dengan sangat hati-hati. Beberapa jenis hidrida yang termasuk dalam golongan ini, antara lain:
(i) Diboran (B$latex _2$H$latex _6$), yaitu gas beracun dan tak berwarna dengan titik leleh -164 $latex ^{\circ}\textrm{C}$ beserta aroma iritatif yang khas. Hidrida ini merupakan bahan reduktor kuat senyawa anorganik dan organik. Bahan ini juga bermanfaat sebagai bahan hidroborasi untuk memasukkan gugus fungsi pada olefin, setelah penambahan olefin beserta reaksinya dengan pereaksi (reagen) yang cocok.
(ii) Amonia (NH$latex _3$), gas beracun dan tak berwarna dengan titik leleh -77,7 $latex ^{\circ}\textrm{C}$ dan disertai dengan bau iritatif yang khas. Gas ini digunakan sebagai larutan amonia dalam air dan pelarut non-air untuk reaksi khusus. Sejak dikembangkannya proses Harber-Bosch untuk sintesis amonia pada tahun 1913, amonia banyak digunakan sebagai bahan baku dalam senyawa yang mengandung nitrogen. Selain itu, amonia juga digunakan sebagai refrigerant dalam lemari pendingin (refrigerator).
(iii) Hidrogen sulfide (H$latex _2$S), gas beracun yang tak berwarna dengan titik leleh -85,5$latex ^{\circ}\textrm{C}$ yang memiliki bau seperti telur busuk. Gas ini digunakan untuk analisis kimia dengan cara pengendapan ion logam dan pembuatan senyawa yang mengandung belerang.
(iv) Hidrogen florida (HF) adalah gas tak berwarna, berasap, bertitik leleh -83$latex ^{\circ}\textrm{C}$ dengan aroma yang mengiritasi. Gas ini biasa digunakan dalam proses preparasi senyawa anorganik dan organik yang mengandung flor. Karena permitivitasnya yang tinggi, senyawa ini dapat pula digunakan sebagai pelarut non-air. Larutan dalam air gas ini disebut asam florat dan disimpan dalam wadah polietilen karena asam ini dapat mengkontaminasi gelas.
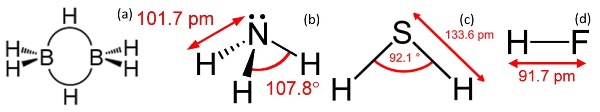
Sumber gambar: http://www.wikipedia.org
3. Hidrida molekular kompleks
Hidrida molekular kompleks merupakan senyawa kompleks yang berkoordinasi dengan ligan hidrida. Logam transisi pada golongan 6 sampai 10 yang tidak membentuk hidrida biner menghasilkan banyak kompleks hidrida dengan ligan tambahan seperti karbonil (CO), fosfin tersier (PR$latex _3$), dan siklopentadietil (C$latex _5$H$latex _5$).
4. Hidrida logam
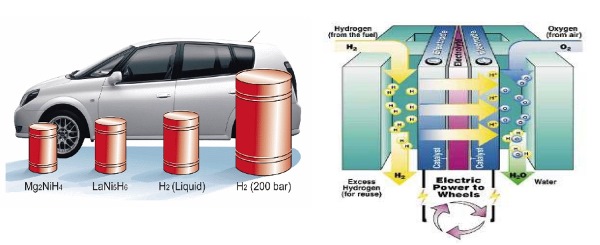
Hidrida MHx yang menunjukkan sifat logam biasanya bersifat non-stoikiometris dan hidrogen menempati lubang dalam kisi logam (interstitial). Hidrida jenis ini yang dikenal meliputi hidrida dari golongan 3 (Sc, Y), golongan 4 (Ti, Zr, Hf), golongan 5 (V, Nb, Ta), Cr, Ni, Pd, dan Cu. Paladium (Pd) dapat bereaksi dengan gas hidrogen pada suhu ruang dan membentuk hidrida yang mempunyai komposisi PdH$latex _x$ ($latex x$ < 1). LaNi$latex _5$ adalah senyawa paduan antara lanthanum dan nikel, yang dapat menampung sampai 6 atom hidrogen per sel satuan dan berubah menjadi senyawa LaNi$latex _5$H$latex _6$. Paduan ini menjadi salah satu kandidat untuk digunakan sebagai bahan penyimpanan hidrogen untuk pengembangan mobil berbahan hidrogen.
Penyimpanan gas hidrogen
Pada saat menjalankan mobil dengan teknologi fuel cell (alat pembangkit listrik yang berasal dari reaksi kimia) berbahan bakar hidrogen kemungkinan akan menjadi tren yang sangat umum di masa mendatang, meskipun untuk saat ini teknologi tersebut masih sedikit diaplikasikan. Hal ini disebabkan karena keterbatasan teknologi penyimpanan gas hidrogen dalam jumlah besar yang aman dan praktis yang dapat dibawa oleh kendaraan. Dalam konteks ini, penyimpanan dengan tekanan tinggi menggunakan tabung dinilai tidak aman sehingga salah satu solusi yang ditawarkan ialah dengan menyimpan hidrogen pada bahan penyerap khusus yang dapat beroperasi pada tekanan rendah.
Beberapa jurnal yang dipublikasikan pada Journal of the American Chemical Society memaparkan suatu lompatan penting dalam teknologi penyimpanan hidrogen berupa pembuktian mengenai kuatnya perekatan H$latex _2$ pada permukaan terbuka atom logam dalam struktur logam-organik nanoporous, bahan berpori yang berukuran pori nanometer, yang disebut dengan MOF (Metal-Organic Framework). Kemampuan dari H$latex _2$ untuk melekat pada atom logam dengan baik memungkinkan molekul hidrogen dapat tersusun lebih padat yang diharapkan dapat meningkatkan kapasaitas penyimpanan dibandingkan dengan penyerapan hidrogen pada material penyerap non-logam yang dikembangkan sebelumnya.
Jeffry Long dari University of California, Berkeley dan timnya telah berhasil mensintesis Mn- Benzenetristetrazolate MOF dengan kapasitas penyimpanan H$latex _2$ sekitar 6,9% berat atau 60 g/L pada suhu 77 K dan tekanan 90 bar. (Dinca, 2006) Untuk saat ini, kapasitas tersebut merupakan kapasitas terbesar untuk bahan MOF dan merupakan bahan yang pertama kali melampaui kapasitas yang ditargetkan oleh Departemen Energi AS yang mencanangkan target penyimpanan hidrogen dengan kapasitas 6,0% dan 45 g/L pada tahun 2010 yang lalu.
Sementara itu, Cameron Kepert dari University of Sydney dan timnya telah berhasil mengembangkan Cu(II)-Tetracarboxylate MOF dengan mempelajari penyerapan deuterium (D$latex _2$) pada bahan tersebut. (Petterson, 2006) Berdasarkan data hasil penelitiannya, mereka mengungkapkan ada enam lokasi penyerapan terpisah dari D$latex _2$ dalam struktur MOF. Pertama, lokasi sekitar atom tembaga, kemudian diikuti dengan lokasi sekitar atom non-logam berpori-pori kecil, kemudian barulah lokasi yang berpori-pori besar. Studi ini berhasil menjelaskan langkah tahapan adisi D$latex _2$ ke dalam struktur MOF yang kemudian membuktikan adanya atom logam dapat menguntungkan penyerapan molekul gas.
Hingga saat ini masih terdapat beberapa kekurangan dari penyimpanan H$latex _2$ dalam struktur MOF, salah satunya ialah lemahnya interaksi atau tarik-menarik antara H$latex _2$ dengan dinding pori dari MOF. Oleh karena itu, para peneliti sekarang berusaha untuk mengatasinya dengan dua cara untuk memperbesar kapasitas penyimpanan, yaitu dengan cara menambah luas permukaan penyerapan MOF atau memperkuat perekatan dari H$latex _2$ sehingga semakin banyak molekul gas hidrogen yang dapat disimpan.
Bahan bacaan:
- http://en.wikipedia.org/wiki/hydride
- M. Dinca, dkk. Hydrogen storage in a Microporous Metal−Organic Framework with Exposed Mn2+ Coordination Sites, J. Am. Chem. Soc. 128, 16876 (2006).
- V. K. Peterson, dkk. Neutron Powder Diffraction Study of D2 Sorption in Cu3(1,3,5-benzenetricarboxylate)2, J. Am. Chem. Soc. 128, 15578 (2006).
Penulis:
Fran Kurnia, mahasiswa S3 di The University of New South Wales, Australia.
Kontak: fran.kurnia(at)yahoo(dot)com



